Inflammatoire
Lewis-Sumner
Pascaud et al. ont repris 145 dossiers Lewis-Sumner collectés sur une période de 15 ans [1]. Seize patients ont présenté un début mono-tronculaire, avec une atteinte initiale touchant préférentiellement le nerf ulnaire (44 %) et un délai de diagnostic de 2 ans. Certains patients ont présenté une généralisation de l’atteinte, d’autres sont restés stables. Le diagnostic de polyradiculonévrite inflammatoire démyélinisante chronique (PIDC) a été posé sur les critères diagnostiques de l’EFNS/PNS :
• 30 % des patients étaient classés en PIDC certaine,
• 50 % en PIDC possible,
• et, chez les 20 % restants, le diagnostic de PIDC a été retenu sur les critères de support.
Dans cette série, les patients traités précocement n’ont pas présenté de généralisation du tableau clinique ou restaient même sur une atteinte mono-tronculaire.
Cette revue souligne que l’utilisation des critères EFNS/PNS permet de confirmer le diagnostic même si l’atteinte est mono-tronculaire et suggère qu’un diagnostic précoce et un traitement instauré rapidement pourraient éviter la généralisation de l’atteinte et, de fait, transformeraient le pronostic fonctionnel de la maladie.
La place de l’imagerie dans la prise en charge de la PIDC
L’équipe italienne de Tozza et al. a fait une revue de littérature sur l’apport de l’échographie nerveuse et de l’IRM dans le diagnostic et le suivi des PIDC, analysant 106 articles : 63 articles pour l’échographie et 43 pour l’IRM [2].
L’échographie
Les protocoles complets d’échographie comprenaient le nerf vague, trois nerfs aux membres supérieurs, trois nerfs aux membres inférieurs, le plexus brachial et l’émergence des racines C5 et C6. Les protocoles simplifiés incluaient médian et racine C5 avec une spécificité de 69 % et une sensibilité de 97 % pour des PIDC validées selon les critères EFNS/PNS. Les paramètres recommandés à l’issue de l’analyse étaient le score UPSS, qui permet d’affirmer une PIDC s’il est ≥ 10 points avec une sensibilité > 85 %, le score BUS (Bilatéral Ultrasond Score), qui distingue PIDC et syndrome de Guillain-Barré (SGB), l’hypertrophie nerveuse diffuse, qui permet de différencier PIDC et Charcot-Marie-Tooth (CMT), l’hyperéchogénicité, qui plaide en faveur de la PIDC, et enfin le Doppler qui pourrait être un marqueur d’activité inflammatoire. De plus, la dimension des fascicules semble diminuer en cas de réponse favorable au traitement.
L’échographie joue donc un rôle déterminant tout à la fois dans le diagnostic, le pronostic ainsi que le suivi des patients.
L’IRM
En IRM, hormis l’aspect typique d’hypersignal T2 (± rehaussé au gadolinium), le plexus lombosacré semble plus sensible et spécifique que le plexus brachial (respectivement 75 et 89 % versus 60 et 82 %). Les auteurs ont proposé le protocole d’étude suivant : le Short Tau Inversion Recovery (STIR) mesurant l’intensité du signal/hypertrophie, la pondération T2 (lésions et inflammation), le tenseur de diffusion (démyélinisation) et l’injection (œdème ou inflammation) permettant ainsi de mesurer l’hypertrophie nerveuse, l’intensité du signal et l’injection (en lien avec l’activité de la maladie).
En analysant tous ces paramètres, les auteurs confirment l’intérêt de l’IRM dans le diagnostic des PIDC, mais elle serait beaucoup moins contributive pour le pronostic et le suivi des patients.
Des avancées complémentaires
La cascade du complément est-elle impliquée dans la démyélinisation et, si oui, y a-t-il une place pour les médicaments anti-complément dans les PIDC ? L’équipe allemande de Stascheit et al. a tenté de répondre à la question [3]. Les auteurs ont repris 55 biopsies de nerf sural de patients atteints de PIDC sur une période de 17 ans. Les patients ont été biopsiés pour des raisons particulières : persistance d’un doute diagnostique, mauvaise réponse au traitement ou encore traitement insuffisant. Toutes les biopsies ont été pratiquées à 6 semaines de traitement (corticoïdes ou immunoglobulines intraveineuses).
Les auteurs ont constaté la présence de dépôts de complexes C5b9 dans 94 % des biopsies, des infiltrats de cellules TCD8, des macrophages ainsi que des signes de démyélinisation en microscopie électronique. Les études protéomiques réalisées chez 10 patients ont objectivé une augmentation de toutes les protéines du complément sur les Volcano-plots, faisant émettre l’hypothèse de l’implication de voies de signalisation médiées par le complément dans l’altération des vaisseaux.
De plus, l’expression de ces dépôts C5b9 semblait corrélée au score INCAT ; 70 % des patients avec une expression haute à modérée avaient une maladie évolutive. L’expression des marqueurs CD8 et CD68 était également corrélée au score INCAT.
Cela suggère que le complément pourrait rentrer dans la cascade de la démyélinisation et représenter un marqueur anatomopathologique pour les futurs essais thérapeutiques.
Le biomarqueur référence
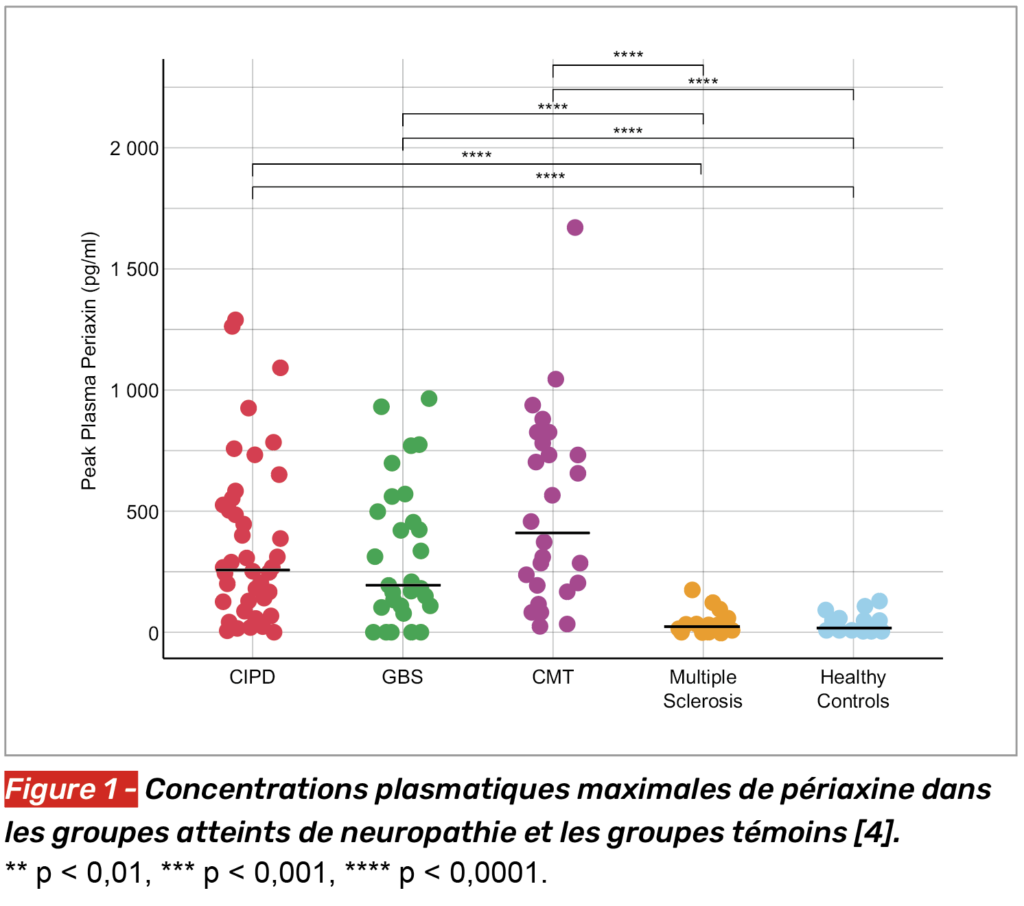
La périaxine est une protéine exprimée par les cellules de Schwann et spécifique du système nerveux périphérique. Son taux plasmatique est augmenté dans les atteintes démyélinisantes et parfois dans certaines atteintes axonales, elle pourrait représenter un biomarqueur de la PIDC. Dans cette étude londonienne, les auteurs ont colligé 45 patients porteurs de PIDC, 30 patients de syndrome de Guillain-Barré (SGB) et 20 de Charcot-Marie-Tooth (CMT), ainsi que 30 contrôles malades (sclérose en plaques) et 30 contrôles sains [4].
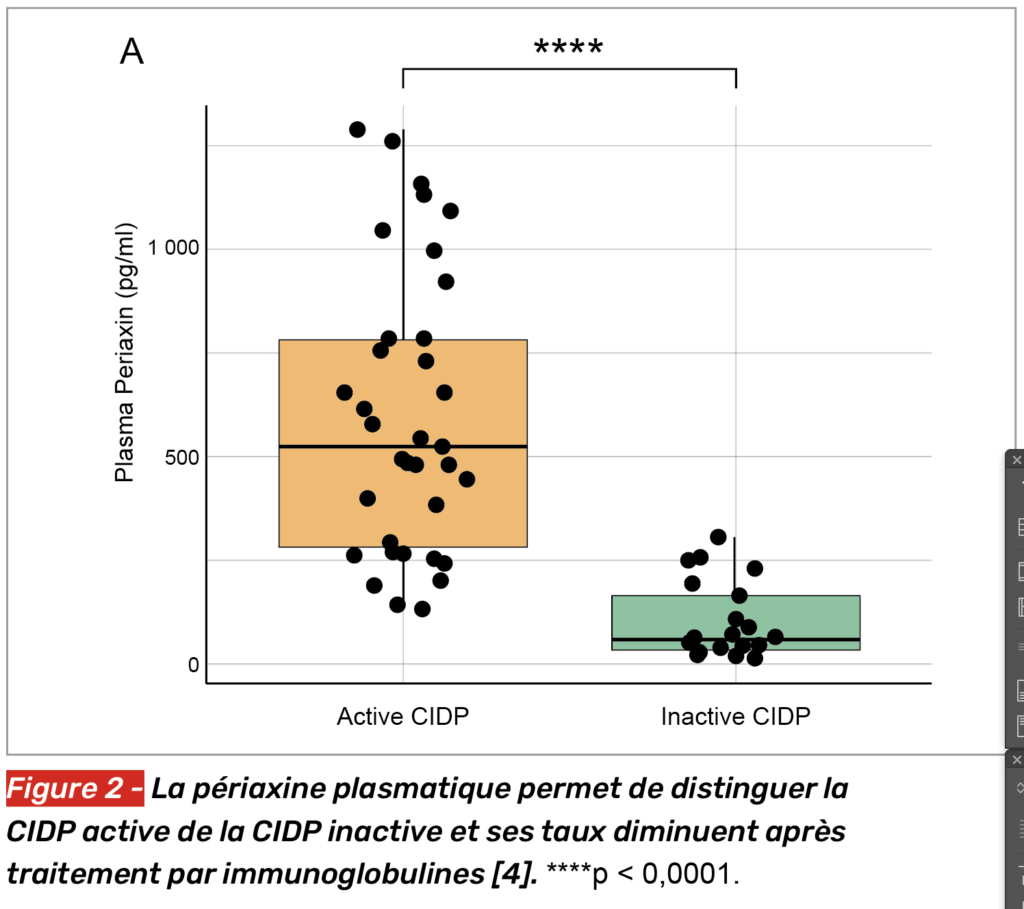
La périaxine est augmentée dans la PIDC, le SGB et le CMT, mais les modifications restent peu significatives chez les contrôles (sains et malades) (Fig. 1). Dans la PIDC, le taux de périaxine atteint en moyenne 240 versus 19,0 et 14,6 pg/ml chez les contrôles (SEP et contrôles sains). Dans les formes actives de PIDC, il atteint même 522 contre 58 pg/ml dans les formes inactives (Fig. 2). Le taux diminuait à 4 semaines de traitement par immunoglobulines intraveineuses, sauf chez deux patients qui avaient présenté une rechute ; il remontait autour de 263 pg/ml chez les patients cliniquement aggravés.
Ces données suggèrent donc que la périaxine pourrait être un marqueur bien utile au monitoring des patients (rechutes et aggravation).
• Kouton L. Le Hit-Parade de la SFNP : inflammatoire. SFNP 2026.
Génétique
Des phénotypes “overlap nerf-muscle”
Se référant au travail publié récemment par une équipe italienne, Marion Masingue a souligné l’existence d’un groupe de gènes responsables de phénotypes “overlap nerf-muscle” caractérisés par l’association, à des degrés variables, d’une atteinte musculaire à une atteinte du nerf périphérique et se présentant parfois sous des formes mixtes difficilement diagnostiquées [5, 6]. Deux profils principaux peuvent être individualisés : un phénotype scapulo-péronéal, observé notamment dans les mutations de LMNA, HSPB3 et BAG3, et un phénotype non longueur-dépendant, typique de certaines atteintes axonales distales associées aux mutations de BICD2, HSPB8, DNM2, MYH14 et VWA1. L’atteinte musculaire prédomine dans les mutations LAMA2, CRYAB ou GNE. En revanche, la neuropathie périphérique est retrouvée dans les mutations HSBP1, SPTAN1 et DNAJB2.
Le gène VCP
Par ailleurs, ce travail a permis d’individualiser le groupe de protéinopathies multisystémiques dues à des variants sur le gène VCP (Valosin-Containing Protein), responsables de phénotypes cliniques complexes associant (ou pas, selon les membres de la famille) neuropathie périphérique type CMT, sclérose latérale amyotrophique, démence fronto-temporale, atteinte myopathique (myosite à inclusions). Depuis son identification, d’autres tableaux liés à ce gène ont été rapportés, responsables de phénotypes encore plus complexes impliquant différentes combinaisons d’atteintes nerf-cerveau-muscle, parfois associées à une atteinte osseuse (Paget).
La physiopathologie de ces phénotypes “overlap” est complexe et reposerait sur l’interaction de mécanismes communs, notamment un déficit énergétique mitochondrial, des altérations de la matrice extracellulaire et un dysfonctionnement de la protéostase. À ces mécanismes s’ajoutent des voies spécifiques à certains gènes, dont l’association peut être synergique ou antagoniste, ce qui expliquerait la variabilité phénotypique observée.
• Masingue M. Le Hit-Parade de la SFNP : génétique. SFNP 2026.
Thérapeutique
Hard Rock et syndrome du canal carpien
Faut-il privilégier la chirurgie aux infiltrations dès que le diagnostic est posé ?
Selon des données de la littérature, la chirurgie à 12 mois est plus efficace que l’infiltration (75 contre 38-61 %). Dans l’étude DISTRICTS de Palmbergen et al. de 2025 [7], le syndrome du canal carpien (SCC) a été confirmé par ENMG dans 67 % des cas, par échographie dans 19 % des cas et en combinant les deux examens dans 15 % des cas. Au total, 468 patients ont été opérés et 466 ont bénéficié d’infiltrations. Le taux de récupération clinique était de 61 % dans le groupe chirurgie contre 45 % dans le groupe infiltration, avec un délai moyen de récupération respectivement de 9 et 18 mois. Si l’amélioration est plus rapide à 6 semaines chez les patients dans le groupe infiltration, ceci s’inverse en faveur d’un bénéfice durable de la chirurgie. L’analyse des paramètres électrophysiologiques et échographiques identifiait peu de facteurs prédictifs discriminants. Toutefois, une différence de latence sensitive médian/ulnaire au 4e doigt > 1 ms était associée à une meilleure réponse à la chirurgie. De même, une surface de section du nerf médian supérieure à 15 mm à l’échographie semblait prédire un bénéfice plus marqué du traitement chirurgical.
Du AC/DC dans les blocs !
Dans une note plus anecdotique, il a été rappelé que les chirurgiens semblent plus fréquemment écouter du Hard Rock que de la musique classique au bloc opératoire. L’étude de Yang et al. de 2022 [8] a montré que l’écoute de musique de type AC/DC était associée à une amélioration des performances et à une réduction du temps opératoire lors de procédures laparoscopiques. Aucune étude n’existe toutefois pour la chirurgie du canal carpien, mais cette observation ouvre une perspective originale qui pourrait mériter d’être explorée.
Les approches conservatrices
Une méta-analyse de 2025 [9] a évalué 11 approches conservatrices du SCC, incluant les infiltrations de corticoïdes, l’immobilisation par orthèse et d’autres thérapies non médicamenteuses. Une technique manuelle combinant traction et immobilisation semblerait la plus efficace. Cependant les résultats doivent être interprétés avec prudence en raison de limites méthodologiques.
Faut-il revoir la stratégie de prise en charge du SCC en se fondant sur les critères ENMG et échographiques ? Quelle serait la place des approches non médicamenteuses dans cette prise en charge ? Les résultats médico-économiques à venir de l’étude DISTRICTS pourront apporter des éléments déterminants pour redéfinir la place des traitements conservateurs dans la prise en charge globale du SCC.
La passion “des douleurs neuropathiques”
La prise en charge de la douleur neuropathique reste un authentique sujet d’actualité.
• Blandine Acket a abordé ce volet en présentant une méta-analyse [10] s’inscrivant dans le prolongement d’un travail publié en 2015 par la même équipe. Elle a porté sur les thérapeutiques pharmacologiques et la neuromodulation non invasive et a inclus 313 études, dont 284 pharmacologiques et 29 de neuromodulation, avec, en critères de sélection, des essais randomisés en double aveugle contre placebo évaluant le traitement médicamenteux ou en neuromodulation, administrés pendant au moins 3 semaines ou avec un suivi minimal d’au moins 3 semaines et au moins 10 patients par groupe. Le critère de jugement principal était la proportion de répondeurs (réduction de 30-50 % de l’intensité de la douleur initiale). Comparativement à la publication de 2015, cette étude renforce l’idée que les α2δ-ligands (gabapentine, prégabaline), les antidépresseurs tricycliques et les IRSNA (duloxétine, venlafaxine) sont bien utilisés en première ligne. L’élément nouveau est l’apparition en seconde ligne de la capsaïcine en topique et de celle de la rTMS en traitement reconnu. En revanche, les opioïdes sont relégués en 3e ligne de traitement en raison de leur effet addictif.
• Une publication [11] souligne également l’émergence de plusieurs techniques de neurostimulation et de neuromodulation susceptibles de prendre une place dans la prise en charge des douleurs neuropathiques.
• Pour revenir à la musique, d’autres approches telles que la musicothérapie [12] pourraient moduler la douleur via les voies dopaminergiques.
CRISPR-Cas9 dans l’amylose héréditaire à transthyrétine (hATTR)
Le traitement précoce de l’amylose héréditaire à transthyrétine (hATTR) est crucial afin de limiter la progression de la maladie et d’éviter l’apparition de nouveaux phénotypes récemment décrits, cérébraux ou ophtalmologiques. L’édition génique via CRISPR-Cas9 fait maintenant partie des outils étudiés dans l’amylose hATTR [13]. Dans l’hépatocyte, Cas9 est exprimée transitoirement, elle coupe l’ADN du gène TTR et le rend non fonctionnel, supprimant ainsi la production hépatique de TTR. Point fondamental pour les cliniciens : quelles différences avec les traitements actuels ? Le tafamidis stabilise la protéine, les siRNA et oligonucléotides antisens bloquent sa production à plus de 90 %, mais de façon réversible. L’édition génique CRISPR-Cas9 permet de la supprimer.
L’étude de phase I
L’objectif de cette étude de phase I, réalisée en ouvert, était d’évaluer la tolérance et la pharmacodynamie du Nexguran Ziclumeran chez les patients présentant une amylose hATTR avec neuropathie. Les objectifs secondaires incluaient le changement dans le stade de la polyneuropathie, le score d’invalidité lié à la polyneuropathie, le taux sérique de neurofilaments, l’IMC modifié et le score mNIS+7. Le traitement a été administré en une perfusion unique des nanoparticules lipidiques contenant un ARN messager codant pour l’enzyme Cas9 et un ARN guide ciblant de façon spécifique le gène TTR.
Les résultats de cette étude étaient prometteurs, avec un taux sanguin de TTR (préalbumine) diminué de 90 %, une stabilité clinique et une amélioration du score de mNIS chez 50 % des patients.
Cette approche thérapeutique innovante de l’édition génique par CRISPR-Cas9 inactive de façon potentiellement définitive le gène TTR, ouvrant la voie à une approche thérapeutique one-shot. Les phases ultérieures devront confirmer l’efficacité de cette approche et sa tolérance à long terme.
• Acket B. Le Hit-Parade de la SFNP : thérapeutique. SFNP 2026.
Bibliographie
1. Pascaud J, Fortanier E, Salort-Campana E et al. Chronic inflammatory demyelinating polyradiculoneuropathies (CIDP) with monotruncular onset: Frequency, clinical features, electrophysiology, and evolution. Eur J Neurol 2025 ; 32 : e16560.
2. Tozza S, Cassano E, Erra C et al. Role of imaging in chronic inflammatory demyelinating polyneuropathy: a systematic review. Eur J Neurol 2025 ; 32 : e70226.
3. Stascheit F, Roos A, Schroeter CB et al. Complement profiling of sural nerves in chronic-inflammatory demyelinating polyneuropathy. Acta Neuropathol 2025 ; 150 : 32.
4. Bellanti R, Keh RYS, Keddie S et al. Plasma periaxin is a biomarker of peripheral nerve demyelination. Brain 2025 ; 148 : 4448-60.
5. Laurini C, Bosco L, Zambon AA et al. Neuromuscular disorders with evidence of both neuropathic and myopathic phenotype. Brain 2025 : awaf399.
6. Benkirane M, Marelli C, Choumert A et al. Type and position of repeat interruption as determinants of disease severity and expansions size in Friedreich ataxia. Genet Med 2025 ; 27 : 101588.
7. Palmbergen WAC, Beekman R, Heeren AM et al. Surgery versus corticosteroid injection for carpal tunnel syndrome (DISTRICTS): an open-label, multicentre, randomised controlled trial. Lancet 2025 ; 405 : 2153-63.
8. Yang C, Möttig F, Weitz J et al. Effect of genre and amplitude of music during laparoscopic surgery. Langenbecks Arch Surg 2022 ; 407 : 2115-21.
9. Chen Y, Han B, Zhang X et al. Conservative treatments of carpal tunnel syndrome: a systematic review and network meta-analysis. Arch Phys Med Rehabil 2025 ; 106 : 1447-58.
10. Soliman N, Moisset X, Ferraro MC et al. Pharmacotherapy and non-invasive neuromodulation for neuropathic pain: a systematic review and meta-analysis. Lancet Neurol 2025 ; 24 : 413-28.
11. Ciampi de Andrade D, Shirvalkar P. The future of pain research: neuromodulation and surgery. Pain 2025 ; 166 : S116-20.
12. Sihvonen AJ, Pitkäniemi A, Särkämö T, Soinila S. Isn’t there room for music in chronic pain management? J Pain 2022 ; 23 : 1143-50.
13. Gillmore JD, Gane E, Täubel J et al. Nexiguran Ziclumeran gene editing in hereditary ATTR with polyneuropathy. N Engl J Med 2025 ; 393 : 1375-86.
L’autrice déclare ne pas avoir de liens d’intérêt en rapport avec cet article.