Les progrès considérables que nous avons vécus ces 30 dernières années concernant la prise en charge thérapeutique de la sclérose en plaques (SEP) et l’importance de l’arsenal thérapeutique qui s’est remarquablement enrichi nous ont conduits à réfléchir et à discuter de l’évaluation des critères d’efficacité de ces traitements, notamment de la réponse thérapeutique. Des critères de réponses thérapeutiques ont ainsi émergé, avec notamment les critères de Rio (ensuite Rio modifiés), puis les critères de MAGNIMS, permettant de juger de la nécessité ou non d’adapter la stratégie thérapeutique, et ceci, de manière précoce. Ces critères nous ont amenés à évoluer vers la nécessité d’un objectif thérapeutique ambitieux, visant à tendre vers l’absence d’évolutivité sur le plan clinique et neuroradiologique, communément appelé “objectif rémission”.
Le NEDA (No Evidence of Disease Activity)
Origine du concept
Ce concept, défini par un critère composite, le NEDA (No Evidence of Disease Activity, ou absence de signe d’activité de la maladie) est né en 2012. Celui-ci a émergé lors de la première réunion « Freedom from MS Disease Activity: what does it mean and how do we achieve it? » qui s’est tenue à la Cleveland Clinic en septembre 2012, organisée par Rob Bermel et Richard Rudick. Au cours de cette réunion, Ted Phillips a fait une présentation intitulée « Statut sans maladie, contrôle complet de la maladie et rémission : que pouvons-nous apprendre d’autres domaines médicaux (par ex. oncologie, gastroentérologie ou rhumatologie) ? » Dans son exposé, Ted Phillips a parlé de l’utilisation des termes NED (No Evidence of Disease : aucune preuve de maladie) et MRD (Minimal Residual Disease : maladie résiduelle minimale) [1].
Ainsi est né le concept de NEDA comme un objectif thérapeutique permettant d’évaluer la réponse au traitement chez les patients atteints de SEP, en particulier la forme rémittente-récurrente (SEP-RR).
Les critères d’évaluation
La version initiale comprenait trois critères :
1. absence de poussée clinique,
2. absence de progression du handicap confirmée (EDSS),
3. absence de nouvelle lésion IRM (en T2 ou prenant le gadolinium).
Si ces trois critères étaient remplis à 1 an, on parlait de NEDA-3. Ce concept a été utilisé dans les essais cliniques pour comparer l’efficacité des traitements, puis adopté en pratique clinique comme indicateur d’une bonne réponse thérapeutique. Pour refléter davantage l’aspect neurodégénératif de la SEP, certains experts ont ajouté un quatrième critère beaucoup plus lié à la neurodégénérescence : absence d’atrophie cérébrale excessive (taux de perte de volume cérébral normalisé). Cette version a surtout été utilisée dans les études, mais beaucoup moins en pratique courante, car la mesure du volume cérébral était techniquement plus complexe, moins standardisée et difficilement quantifiable à l’échelon individuel.
Les limites
Malgré son utilité, plusieurs limites au NEDA ont été identifiées.
• Le caractère très strict de ce concept (beaucoup de patients sortent du NEDA après de petites anomalies IRM sans traduction clinique).
• Par ailleurs, le NEDA ne reflète pas toujours la progression silencieuse de la maladie.
• Le maintien durable du NEDA est difficile et rare au-delà de 2-3 ans selon les études.
• Il ne prend pas en compte les troubles cognitifs, souvent importants dans la SEP.
Ainsi, d’autres auteurs ont proposé de rajouter d’autres dimensions permettant d’être certains de l’absence d’activité de la maladie (acuité visuelle bas contraste, qualité de vie…). On a parlé de NEDA-4 puis de NEDA-5.
Malgré ses limites, le NEDA a très nettement contribué à l’objectif thérapeutique dit de traitement précoce et efficace. Il a renforcé l’idée de cibler une activité inflammatoire minimale. Il a aidé à comparer les médicaments dans les essais cliniques. Il demeure aujourd’hui un indicateur utile pour guider seul la prise en charge. Le NEDA est adopté dans les discussions sur l’optimisation thérapeutique, mais également dans les recommandations de monitoring.
Le MEDA (Minimal Evidence of Disease Activity)
Compte tenu du caractère très strict et restreint pour obtenir un NEDA, d’autres auteurs ont proposé le concept de MEDA (Minimal Evidence of Disease Activity), objectif plus facile à tenir en pratique courante.
Les critères
Plusieurs définitions du statut MEDA ont été proposées.
• Dans la publication de Rio [2], les auteurs ont défini le statut MEDA comme une activité clinique minime isolée (poussée sans séquelles), une activité IRM minime isolée (une ou deux nouvelles lésions T2 ou une lésion Gd+) ou une activité clinique et IRM minime (une poussée + une nouvelle lésion T2) durant la première année de traitement.
• Dans la publication de Sormani [3], le statut MEDA est aussi défini par un score MAGNIMS faible (absence de poussée et présence d’une activité IRM minimale ≤ deux nouvelles lésions T2).
En pratique
Dans notre pratique, à défaut de consensus, la survenue d’une seule poussée isolée au cours de la première ou la deuxième année de traitement, si elle est rapidement résolutive et sans séquelles, ne nécessite pas systématiquement une adaptation thérapeutique et peut ainsi être considérée comme une activité minimale acceptable. Il en est de même pour un seuil de lésions T2 ≤ (en dehors du tronc cérébral et de la moelle). De plus, comme l’activité IRM est généralement plus fréquente que l’activité clinique, un suivi supplémentaire et une réévaluation du patient sont nécessaires avant d’envisager une escalade thérapeutique.
Si les critères de réponse thérapeutique concernant l’activité inflammatoire sont assez bien définis par le NEDA ou le MEDA, l’évaluation de la progression reste un problème majeur. En effet, jusque-là, cette évaluation ne se référait qu’à l’EDSS (Expanded Disability Status Scale), qui est un score certes incontournable, mais qui a de sérieuses limites (n’évalue que les capacités d’ambulation, n’est pas linéaire, a une grande variabilité inter-individuelle). Ainsi sont apparus plusieurs concepts dans les années qui ont suivi, notamment l’émergence de scores composites.
Le NEP (No Evidence of Progression)
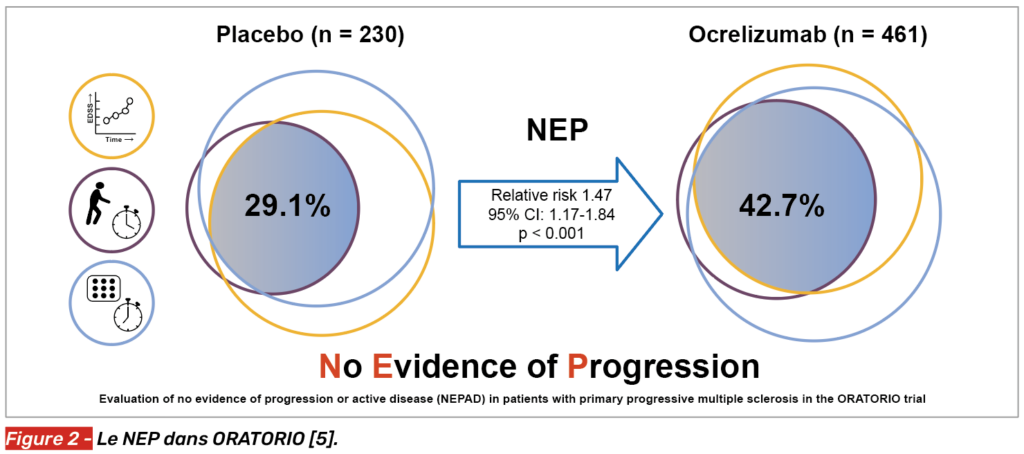
Il s’agit d’un score composite combinant trois évaluations : l’EDSS, le 9 Hole Peg Test (9-HPT) et le Time 25 foot Walk (TW25), initialement proposé dans l’étude PROMISE (Fig. 1) [4].
Les critères
Il était défini par :
• l’absence de progression confirmée sur 12 semaines d’au moins 1 point sur l’échelle EDSS si le score initial était respectivement ≤ 5,5 ou de ≥ 0,5 point si l’EDSS est > 5,5 points ;
• l’absence de progression confirmée sur 12 semaines d’au moins 20 % au TW25 et au 9-HPT.
Ce critère d’évaluation a été repris dans l’essai ORATORIO (ocrélizumab versus placebo dans une population de SEP-PP) dans une étude post-hoc (Fig. 2) [5].
Le NEPAD (No Evidence of Progression and Active Disease)
Par rapport au NEP, ce concept introduit l’évaluation de l’activité IRM.
Les critères
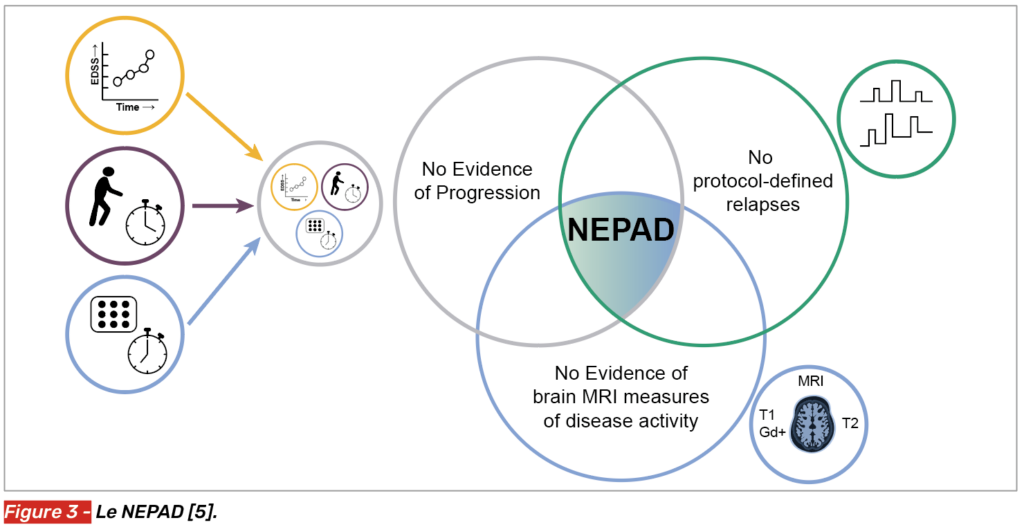
Ainsi, il est défini par (Fig. 3) :
• l’absence de progression confirmée sur 12 semaines d’au moins 1 point sur l’échelle EDSS si le score initial était respectivement ≤ 5,5 ou de ≥ 0,5 point si l’EDSS est > 5,5 points ;
• l’absence de progression confirmée sur 12 semaines d’au moins 20 % au TW25 et au 9-HPT ;
• l’absence d’activité IRM (nouvelles lésions T2 ou majoration de celles-ci ou activité Gado+).
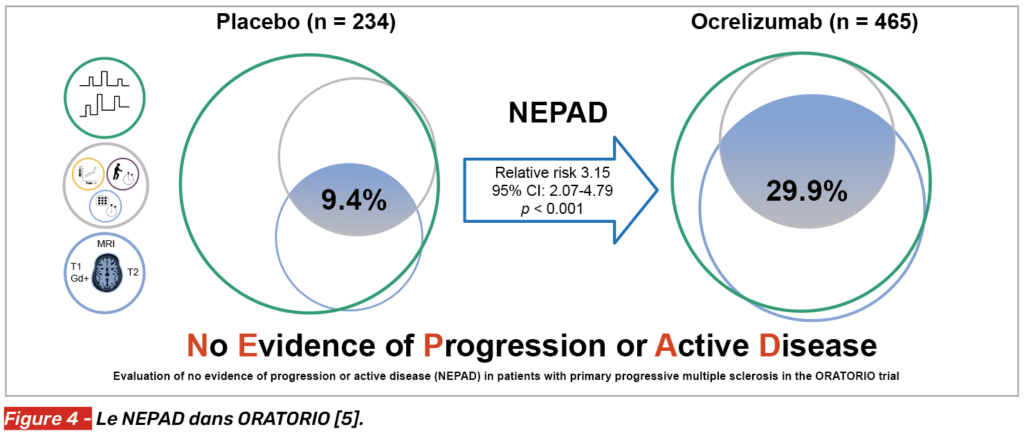
De la même manière, ce critère d’évaluation a été repris dans l’essai ORATORIO (ocrélizumab versus placebo dans une population de SEP-PP) (Fig. 4) [5].
Le PIRA (Progression Independent of Relapse Activity)
À partir des années 2010, plusieurs grandes cohortes (MSBase, EPIC, ORATORIO) ont mis en évidence qu’une part significative de l’aggravation du handicap chez les patients SEP-RR n’était pas liée aux poussées, même lorsqu’ils étaient traités. Ainsi, on parlait de progression chez des patients sans aucune activité inflammatoire visible (poussées ou nouvelles lésions à l’IRM).
Les critères
Entre 2017 et 2022, plusieurs articles majeurs [6, 7] ont défini le PIRA comme suit :
• augmentation du score EDSS (augmentation de 1 point ou de 0,5 point si EDSS > 5,5) ;
• ou augmentation de plus 20 % du T25FW ;
• ou augmentation de plus de 20 % du score du 9-HPT, confirmée à 12 ou 24 semaines.
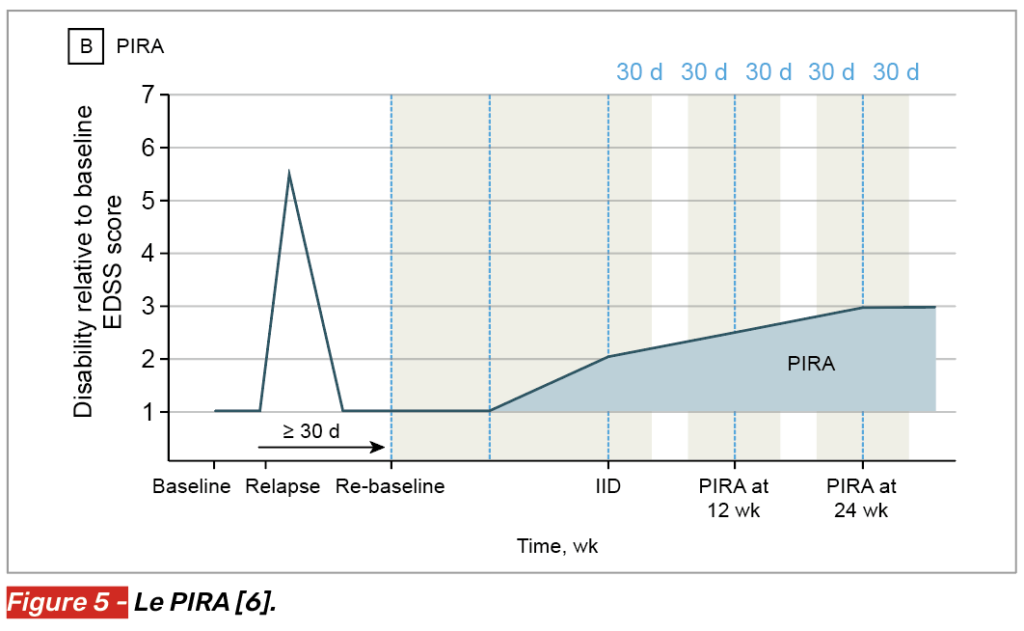
Les scores EDSS/T25FW/9-HPT étaient évalués indépendamment des poussées selon le schéma décrit dans la figure 5.
Intérêt
De nombreuses études ont confirmé que :
• le PIRA représentait la majorité de la progression du handicap dans la SEP-RR (souvent > 70 %) [8-10] ;
• le PIRA commençait dès les premières années, parfois dès le diagnostic ;
• le PIRA était associé à :
- une atrophie cérébrale (surtout substance grise et thalamus),
- un vieillissement du système immunitaire,
- des lésions chroniques actives (smouldering lesions) [11, 12].
Ceci a conduit à modifier nos concepts physiopathologiques, confirmant la co-existence très précoce d’une inflammation aiguë ou focale (poussées cliniques et activité radiologique) et d’une inflammation chronique dite “compartimentalisée” (microglie, lésions bordées actives) [13]. Le PIRA a donc contribué à remettre en cause la vision strictement duale SEP-RR/SEP-SP, à souligner la nécessité de traiter tôt et fort [14], à développer des thérapies ciblant la neurodégénérescence et l’inflammation chronique.
En pratique
Ce critère a été utilisé en post-hoc dans les études poolées OPERA I et II (ocrélizumab versus interféron dans des formes RR de SEP). Depuis 2020 environ, presque tous les essais cliniques incluent des analyses de PIRA. Le PIRA est un endpoint important pour mesurer l’effet des traitements sur la progression silencieuse. Il peut être utilisé en pratique clinique pour détecter un changement de phénotype ou un besoin thérapeutique.
Dans un souci d’uniformisation d’évaluation du PIRA [15, 16], deux articles importants ont discuté de la méthodologie à adopter sur la définition et la fiabilité du PIRA comme critère d’évaluation.
Ainsi, une progression est considérée comme PIRA confirmée s’il y a une aggravation clinique objectivée (sur la base de l’EDSS), persistante ≥ 3 à 6 mois, en l’absence de poussée clinique dans les 90 jours précédents ou les 30 jours suivant l’évaluation clinique, en l’absence de corticothérapie récente, en l’absence d’infection intercurrente, fièvre, fatigue majeure.
Les limites
L’une de ses principales limites réside dans son lien relativement faible avec les processus biologiques sous-jacents qui déterminent la progression de la maladie. Bien que l’échelle PIRA repose sur des mesures cliniques de l’aggravation du handicap, elle ne reflète pas nécessairement la complexité des mécanismes pathologiques impliqués, tels que la neuro-
dégénérescence, l’inflammation chronique ou l’activité immunitaire compartimentée au sein du système nerveux central.
L’autre limite est que le PIRA n’inclut pas de critères d’évaluation radiologique, ce qui ne permet pas d’exclure formellement une progression indépendante des poussées, mais avec une activité radiologique persistante. On a souvent parlé de PIRA dit “actif” lorsque les données IRM retrouvaient une inflammation focale (versus PIRA “non actif” en l’absence d’anomalie IRM pouvant témoigner d’une inflammation focale correspondant à une progression en rapport avec un mécanisme uniquement lié à une inflammation chronique ou “compartimentalisée”).
D’où la naissance du PIAA (Progression Independent of Any Activity) ou PIRMA (Progression Independant of Relapse or MRI Activity).
Le PIRMA (Progression Independent of Relapse or MRI Activity)
Le PIRMA vise à isoler la progression purement dégénérative, en excluant toute participation inflammatoire évidente sur les données de l’IRM. Il cherche à n’évaluer que la progression liée à des mécanismes chroniques (inflammation compartimentalisée, activation de la microglie, lésions lentement évolutives ou smouldering lesions : SEL et/ou PRL, atrophie cérébrale).
Ce concept est important, car il tente d’identifier la progression autonome, indépendante de toute activité inflammatoire visible, ce qui est crucial pour mesurer les effets neuroprotecteurs des traitements, pour définir précocement les formes progressives et pour comprendre la neurodégénérescence dans la SEP.
Ainsi, on en arrive au concept de SAW (Smouldering-Associated Worsening)
Le SAW résume l’aggravation progressive et insidieuse de la maladie, liée à une activité inflammatoire chronique, excluant la participation inflammatoire de la maladie. Cette progression lente et continue reflète des processus pathologiques persistants (lésions chroniques actives, neurodégénérescence).
Ainsi, G. Giovannoni posait déjà la question de savoir si, finalement, cette progression lente ne pouvait pas être le marqueur principal de la maladie, comme en témoigne le titre de cet article : Smouldering multiple sclerosis : the « real MS » [17].
Physiopathologie
Sur le plan physiopathologique, le SAW est associé :
• aux lésions chroniques actives (smouldering lesions) avec inflammation persistante en bordure des plaques,
• à une activation chronique de la microglie,
• à la dégénérescence axonale et neuronale progressive,
• à l’inflammation compartimentée au sein du système nerveux central.
Ce concept est particulièrement important dans la SEP, où il permet d’expliquer la progression du handicap en l’absence de poussée, notamment dans les formes progressives, mais aussi dès les phases précoces de la maladie. Ce concept de SAW est très important si on raisonne sur l’évaluation de stratégies thérapeutiques ciblant exclusivement les mécanismes inflammatoires chroniques et neurodégénératifs responsables de la progression à long terme.
Les limites
L’une des principales limites du SAW réside dans la difficulté à distinguer la progression du handicap lié au vieillissement physiologique de celle liée à une inflammation chronique et compartimentée. Ces deux processus peuvent coexister et engendrer des trajectoires cliniques similaires, mais seule la seconde représente un mécanisme pathologique, potentiellement modifiable. En l’absence de biomarqueur validé permettant de différencier ces voies de manière individuelle, le SAW demeure un outil cliniquement pragmatique mais biologiquement imparfait.
Une déclaration de consensus
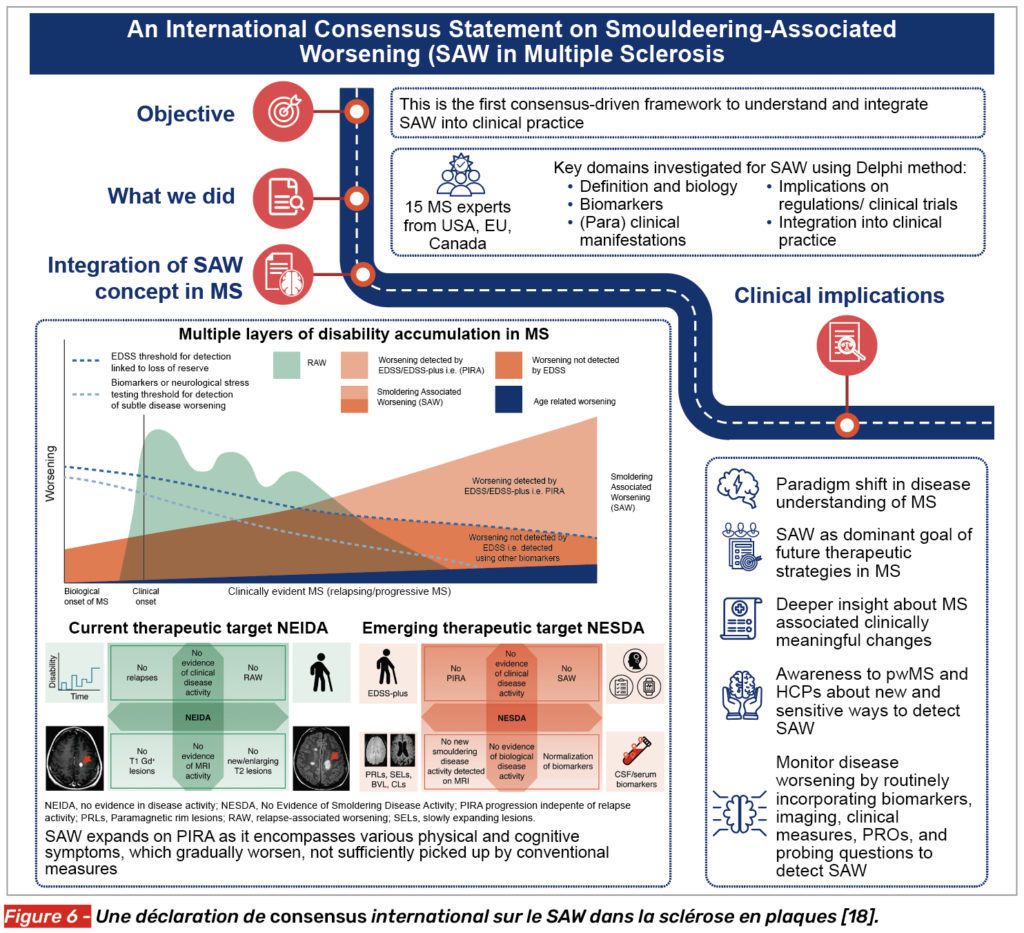
Ainsi, l’évolution des critères d’évaluation d’une stratégie thérapeutique a récemment fait l’objet d’un consensus de 15 experts nord-américains (Fig. 6) [18]. Scalfari et al. [18] proposent maintenant de raisonner sur la base de la double évaluation : inflammation et progression (comme le proposaient les critères de Lublin) avec deux nouveaux concepts.
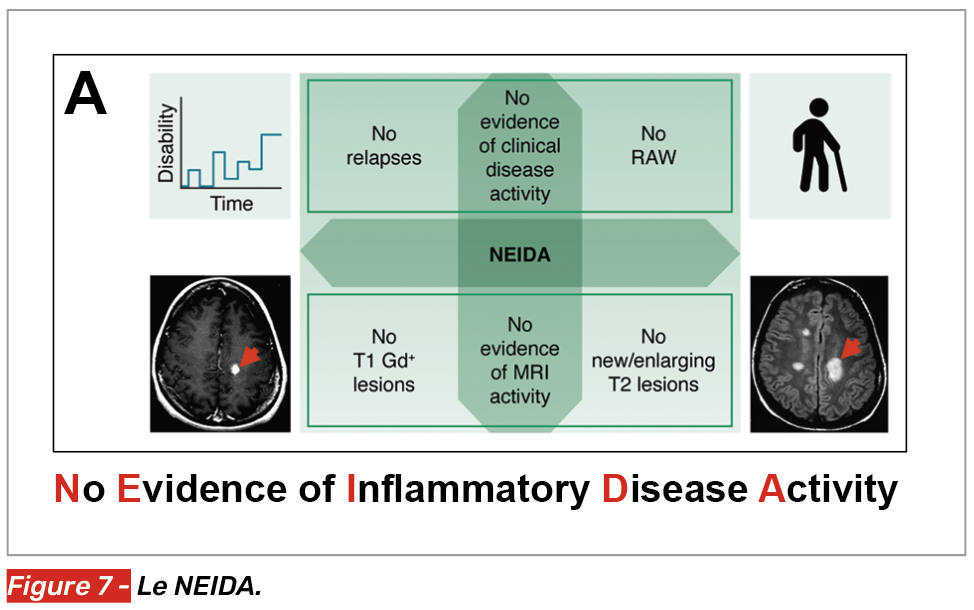
Le NEIDA (No Evidence of inflammatory disease activity) (Fig. 7)
Le NEIDA est défini par :
• l’absence de poussée clinique,
• l’absence de progression liée aux poussées,
• l’absence de prise de contraste à l’IRM,
• l’absence de nouvelles/augmentation de volume de lésions T2.
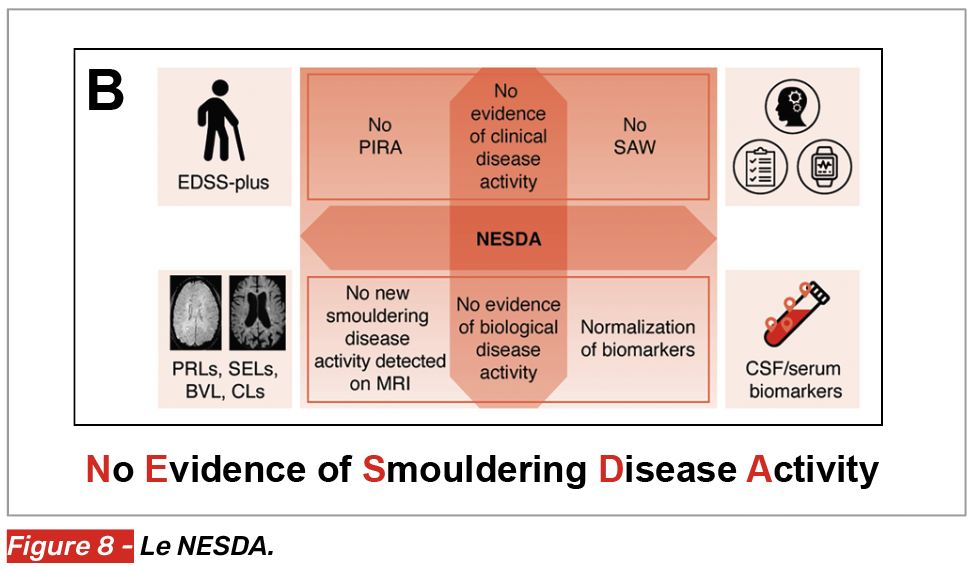
Le NESDA (No Evidence of smouldering disease activity) (Fig. 8)
Le NESDA est défini par :
• l’absence de PIRA,
• l’absence de SAW,
• l’absence de lésions IRM témoignant d’un processus de smouldering disease activity (SEL ; PRL ; lésions corticales ; mesure d’atrophie),
• la normalisation de biomarqueurs biologiques (NfL ; GFAP ; CHI3L ; CXCL13).
Ce NESDA pourrait être à l’avenir un objectif intégré à l’évaluation de molécules visant à étudier l’efficacité sur la progression de la maladie, sachant qu’en pratique il paraît difficile à mettre en place. Les auteurs proposent également d’y adjoindre des tests cognitifs, des scores de fatigue issus de PRO (Patient Reported Outcomes).
Conclusions
Pour ma part, cette dernière proposition paraît parfaitement bien coller d’une part aux différents mécanismes physiopathologiques de la SEP, à notre pratique clinique, notamment au fait que cette évaluation doit être double et dissociée (inflammation et progression). Par ailleurs, il s’agit de critères d’évaluation à prendre en compte lorsqu’on étudie l’effet de molécules sur des cibles différentes. Ainsi, cela amène à réfléchir sur les critères de jugement de l’efficacité d’une molécule dans le cadre d’essais thérapeutiques. Si la clinique et l’IRM restent, de fait, le gold standard pour l’évaluation de l’effet d’une molécule sur l’inflammation, les essais concernant des molécules ciblant la progression devraient avoir pour critère principal le SAW en ciblant le NESDA (il ne faut plus se contenter de l’EDSS ou de scores composites souvent très grossiers pour évaluer cette progression).
L’auteur déclare ne pas avoir de liens d’intérêt en rapport avec cet article.
Bibliographie
1. Giovannoni G, Bermel R, Phillips T, Rudick R. A brief history of NEDA. Mult Scler Relat Disord 2018 ; 20 : 228-30.
2. Rio J, Rovira A, Tintoré M et al. Disability progression markers over 6-12 years in interferon-beta-treated multiple sclerosis patients. Mult Scler 2018 ; 24 : 322-30.
3. Prosperini L, Mancinelli C, Haggiag S et al. Minimal evidence of disease activity (MEDA) in relapsing-remitting multiple sclerosis. J Neurol Neurosurg Psychiatry 2020 ; 91 : 271-7.
4. Koch MW, Cutter GR, Giovannoni G et al. Comparative utility of disability progression measures in PPMS Analysis of the PROMiSe data set. Neurol Neuroimmunol Neuroinflam 2017 ; 4 : e358.
5. Wolinsky J, Montalban X, Hauser SL et al. Evaluation of no evidence of progression or active disease (NEPAD) in patients with primary progressive multiple sclerosis in the ORATORIO trial. Ann Neurol 2018 ; 84 : 527-36.
6. Kappos L, Wolinsky JS, Giovannoni G et al. Contribution of relapse-independent progression vs relapse-associated worsening to overall confirmed disability accumulation in typical relapsing multiple sclerosis in a pooled analysis of 2 randomized clinical trials. JAMA Neurol 2020 ; 77 : 1132-40.
7. Cree BAC, Hollenbach JA, Bove R et al. Silent progression in disease activity–free relapsing multiple sclerosis. Ann Neurol 2019 ; 85 : 653-66.
8. Portaccio E, Bellinvia A, Fonderico M et al. Progression is independent of relapse activity in early multiple sclerosis: a real-life cohort study. Brain 2022 ; 145 : 2796-805.
9. Bayas A, Schuh K, Christ M. Self-assessment of people with relapsing-remitting and progressive multiple sclerosis towards burden of disease, progression, and treatment utilization-Results of a large-scale cross-sectional online survey (MS Perspectives). Mult Scler Relat Disord 2022 ; 68 : 104166.
10. Kappos L, Butzkueven H, Wiendl H et al. Greater sensitivity to multiple sclerosis disability worsening and progression events using a roving versus a fixed reference value in a prospective cohort study. Mult Scler 2018 ; 24 : 963-73.
11. Bozin I, Ge Y, Kuchling J et al. Magnetic resonance phase alterations in multiple sclerosis patients with short and long disease duration. PLoS One 2015 ; 10 : e0128386.
12. Filippi M, Preziosa P, Barkhof F et al. Diagnosis of progressive multiple sclerosis from the imaging perspective: a review. JAMA Neurol 2021 ; 78 : 351-64.
13. Hauser SL, Cree BAC. Treatment of multiple sclerosis: a review. Am J Med 2020 ; 133 : 1380-90.
14. Giovannoni G, et al. Understanding PIRA: implications for early treatment. Mult Scler J 2023.
15. Müller J, Cagol A, Lorscheider J et al Harmonizing definitions for progression independent of relapse activity in multiple sclerosis: a systematic review. JAMA Neurol 2023 ; 80 : 1232-45.
16. Portaccio E, Betti M, De Meo E et al. Toward a unified definition of progression independent of relapse activity in multiple sclerosis. Neurology 2025 ; 105 : e213977.
17. Giovannoni G, et al. Smouldering multiple sclerosis : the « real MS ». Ther Adv Neurol Disord 2022 ; 15 : 17562864211066751.
18. Scalfari A, Traboulsee A, Oh J et al. Smouldering-associated worsening in multiple sclerosis: an international consensus statement on definition, biology, clinical implications, and future directions. Ann Neurol 2024 ; 96 : 826-45.